|
物质 |
C(s) |
CO(g) |
H2(g) |
|
燃烧热 | -393.5 | -283 | -286 |
已知:
写出 与
生成
和
的热化学方程式。
①据图可知,该反应为(填“放热”“吸热”)反应;对该反应的反应速率影响最大的基元反应方程式为。
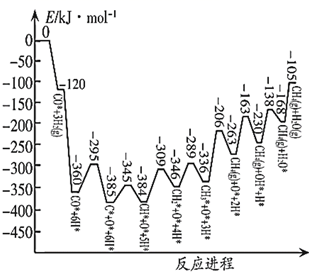
②化学反应速率方程中各物质浓度的指数称为各物质的反应级数,反应级数越大,表示该物质浓度对反应速率影响越大。该反应的反应速率及反应级数随温度变化如图所示

据图可知,为提高反应速率,适宜的反应条件为;温度再高反应速率大幅度降低的原因可能为。
i.
ii.
①升高温度, 的含量增大的原因是。
②恒温恒压密闭容器中,加入 和
,初始压强为
,在
发生反应,反应达平衡时,
的转化率为50%,容器体积减小25%,则反应i的压强平衡常数
(结果保留1位小数)。