 织布 B .
织布 B .  耕田 C .
耕田 C .  生火 D .
生火 D .  灌溉
灌溉 



 B .
B .  C .
C .  D .
D . 
“电解法”证明水的组成(装置如图 1 所示,电极不与水及生成的气体反应)

①通电时发生反应的文字或符号表达式为;
②a、b 两管产生气体的体积比是;
③列关于电解水的说法中正确的是 (填字母)。
a.实验后a 管产生的气体能燃烧
b.该实验中水分子本身不变,改变的是水分子间的间隙
c.该反应属于分解反应
①自来水厂净水的过程中不包括的净水方法是;
a.沉降 b.吸附 c.蒸馏 d.消毒
②河水中的难溶性杂质,可通过过滤的方法除去。用下图装置对河水水样进行过滤,下列关 于过滤的说法中正确的有(填字母);

a.实验中用玻璃棒在漏斗中轻轻搅动以加快过滤速度
b.滤纸边缘需低于漏斗边缘
c.漏斗下端尖嘴需紧靠烧杯内壁
d.若滤纸与漏斗间留有气泡,则会使过滤所得的液体浑浊
e.利用过滤操作,可以将河水中的色素分离出来
③若要检验过滤后的液体是否为硬水,可以取样于试管中加入搅拌后,观察现象。家庭中常用方法将硬水转化为软水,该方法会使家中水壶中产生水垢(主要成分:碳酸钙),家庭中可用(填一种调味品名称)除去水壶内壁上的水垢。
①天然水污染的来源有(请任写一种);
②保护水资源是我们全人类义不容辞的责任。作为一名中学生,我们能为保护水资源作出的努力有(请任写一种具体做法)。

①实验室可选用 D 装置收集 O2的原因是,氧气收集满的现象是;
②集满 O2的集气瓶应正放在实验桌上,原因是;
①若选用 E 装置收集 CO2 , 则气体从端通入(填“a”或“b”),验满的操作是;
②若用该装置验证二氧化碳与水的反应,瓶中需装入(填名称),气体从端通入(填“a”或“b”), 发生反应的文字或符号表达式为。
|
实验序号 |
双氧水溶度 |
双氧水体积(mL) |
温度(℃) |
MnO2 用量(g) |
收集时间(s) |
|
① |
5% |
20 |
20 |
0.2 |
11 |
|
② |
30% |
20 |
20 |
0.2 |
2 |
|
③ |
30% |
20 |
40 |
0 |
148 |
|
④ |
30% |
20 |
90 |
0 |
82 |
①的基础上再增加一组对比实验,小华认为无需增加,将实验②、④进行对比也可得出结论。你的观点是 (填“需要”或“不需要”)增加,理由是。
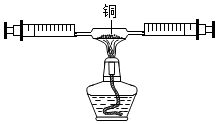
上述反应的文字或符号表达式为。
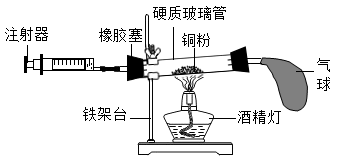
【实验步骤】
具体实验步骤有:
①在硬质玻璃管中装入铜粉,两端塞上带导管的橡皮塞,其中一端用气球密封;
②测量出实验所用硬质玻璃管的体积;
③停止加热后,待试管冷却至室温,注射器活塞稳定后,记录注射器中气体的体积;
④用酒精灯在铜粉部位加热,加热时不断推拉注射器;
⑤移动注射器活塞,在注射器中留下一定体积的气体,记录体积后与硬质玻璃管另一 端密封连接,并将其固定在铁架台上。
正确的操作步骤为(填数字序号);
实验 小组 | 硬质玻璃管的容积/mL | 反应前注射器中气体体积/mL | 反应后注射器中气体体积/mL | 反应消耗的氧气体积/mL | 空气中氧气的体积分数(%) |
甲 | 45 | 15 | 4 | 11 | 18.3 |
乙 | 40 | 18 | 5 | 13 | 22.4 |
丙 | 50 | 20 | 6 |
填写上表中空白,帮助丙组同学完成实验数据的统计。
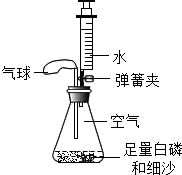
【查阅资料】白磷燃烧所需的最低温度(也叫着火点)为40℃。
【实验准备】锥形瓶内空气体积为 250mL,注射器中水的体积为60mL,该装置气密性良好。
【实验探究】装入药品,按如图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
【现象分析】将锥形瓶底部放入热水中,白磷被引燃,白磷燃烧时产生大量白烟并放出热量;
在整个实验过程中,可观察到气球的变化是(填字母)
A.变小 B .变大 C.先变小后变大 D.先变大后变小
待白磷熄灭,锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:
①注射器中的水自动喷射出来;
②当注射器中的水还剩约时停止下流。
在锥形瓶底铺一层细沙的作用是防止 。
【得出结论】。