 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 点燃酒精灯
C . 点燃酒精灯  D . 检查装置气密性
D . 检查装置气密性 
 ( )
( )

A.化学与生活 | B.化学与环境 |
①生活中常用加热煮沸的方法软化硬水②用燃烧的方法区分羊毛和涤纶 ③利用洗洁精的乳化作用去除油污 | ①焚烧植物秸秆不会造成空气污染 ②PM2.5是造成雾霾天气的原因之一 ③含磷洗涤剂的使用会导致水污染 |
C.化学与安全 | D.化学与健康 |
①炒菜油锅着火可以用锅盖盖灭 ②在室内放一盆水,可防止煤气中毒 ③夜间发现液化气泄漏开灯寻找泄漏源 | ①人体缺铁会引起贫血 ②用甲醛的水溶液浸泡海产品保鲜 ③食用蔬菜和水果来补充维生素 |
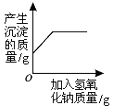 B . 向一定量的稀盐酸中加入铁粉
B . 向一定量的稀盐酸中加入铁粉  C . 稀释pH =2的稀硫酸
C . 稀释pH =2的稀硫酸  D . 氢氧化钠溶液中滴加盐酸
D . 氢氧化钠溶液中滴加盐酸 
①相对分子质量最小的氧化物是;②农业上用来降低土壤酸性的是;
③可用于金属表面除锈的是;④厨房用的酸性调味品是。

①碳棒可用作干电池的电极,说明石墨具有性。
②氯化锌中阴离子的符号是。
③将回收的废旧电池进行分离可以得到二氧化锰,二氧化锰中锰元素的化合价是。实验室用过氧化氢溶液和二氧化锰制取氧气,二氧化锰起作用。

【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3。
实验操作 | 实验现象 | 实验结论 |
①取少量样品于试管中,。 | 有气体产生,气体使石灰水变浑浊。 | 猜想2成立 |
②在上述反应后试管中加少量。 | 。 |

【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
m=.